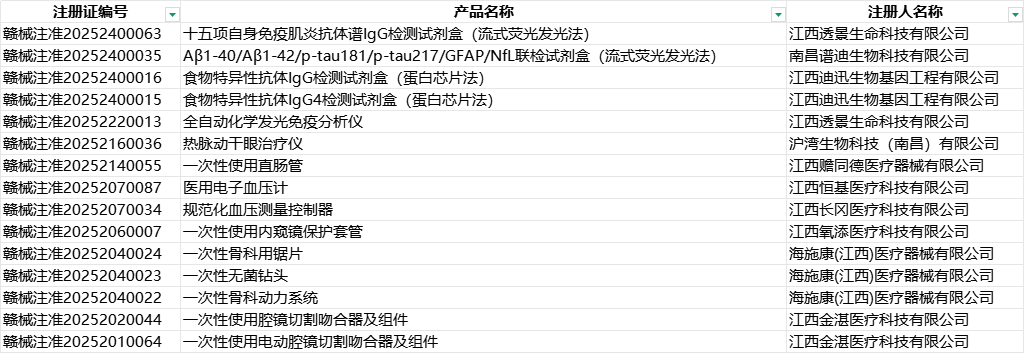
一、数据总览:
2025年上半年,江西省医疗器械注册人制度实施成效显著,共有15项二类医疗器械产品通过注册人制度获批上市,涵盖体外诊断试剂(4项)、医疗设备(4项)及医用耗材(7项)三大类别。这一数据反映出江西省在深化医疗器械审评审批制度改革、鼓励产品创新、优化资源配置方面取得了积极进展。
二、区域产能地图
从注册人分布来看,南昌市(特别是高新技术产业开发区)是医疗器械企业的主要聚集地,进贤县作为传统医疗器械产业基地也持续发力,赣江新区、上饶、抚州等地也有企业分布。
这种区域分布表明江西省医疗器械产业已初步形成集群效应,特别是在南昌高新区,已聚集多家生物医药与医疗器械企业,涵盖试剂、设备等多个细分领域。注册人作为产品上市许可持有人,承担产品质量主体责任,而生产过程则委托给具备相应资质和生产条件的企业完成,这种模式有效促进了跨区域产业协作。江西本地注册人充分利用上海、浙江、江苏、广东等沿海地区的先进制造能力,整合产业链优质资源。例如:江西透景生命科技有限公司集团内委托上海透景诊断科技有限公司生产自身免疫肌炎抗体谱检测试剂盒;江西迪迅生物基因工程有限公司集团内委托杭州浙大迪迅生物基因工程有限公司生产食物特异性抗体检测试剂盒;江西金湛医疗科技有限公司集团内委托常州企业生产腔镜切割吻合器及其组件。
从产品类型分布来看,上半年获批的15项产品中:
IVD产品4项:均采用高新技术平台,如流式荧光发光法、蛋白芯片法等;医疗设备4项:包括全自动化学发光免疫分析仪、热脉动干眼治疗仪、电子血压计及规范化血压测量控制器;医用耗材7项:涵盖内镜、骨科、腔镜手术等多个高值领域。这种多元化的产品结构表明江西医疗器械产业正在向多领域、专业化方向发展,企业市场定位更加精准。
注册人制度为技术创新提供了良好环境,多家企业推出了具有较强竞争力的产品:
IVD领域创新突出:
南昌谱迪生物科技的神经标志物联检试剂盒可同时检测6种阿尔茨海默病相关标志物;
江西透景生命的自身免疫肌炎抗体谱检测试剂盒采用流式荧光法实现多指标并行检测;
迪迅生物的食物特异性抗体检测试剂盒通过蛋白芯片技术实现多靶点同步筛查。
医疗设备领域智能化特征明显:
全自动化学发光免疫分析仪具备样本管理、传输和暂存功能;
规范化血压测量控制器配备摄像头、触摸显示屏和控制软件,实现规范化测量。
医用耗材领域向高端化发展:
电动腔镜吻合器结构复杂,实现电动化控制;
骨科动力系统可实现钻孔、锯切等多种功能。
2025年上半年注册人制度下,医疗器械注册人制度的实施为江西省医疗器械产业创新发展提供了新机遇。通过持续优化制度环境、加强跨区域协作、提升产品质量,江西省有望在中部地区医疗器械产业格局中占据更重要的位置,为公众健康提供更多优质医疗器械产品。注:本报告数据均来自江西药监局2025年1-6月注册批件,旨在为行业提供参考和洞察。
了解器械MAH制度,必须关注MAH小灵通,从此不再走弯路,不被忽悠。